Termodinamika
Oleh Stephanus XI IPA1
A. Pengertian
Termodinamika adalah cabang fisika yang mempelajari tentang kalor dan usaha mekanik pada suatu system (contoh : gas)

Salah satu penerapan konsep termodinamika dalam teknologi
Kesetimbangan kalor terjadi jika tidak ada pertukaran kalor antara kedua benda tersebut saat bersentuhan. Kondisi ini hanya dapat dicapai jika suhu kedua benda tersebut sama.
B. Besaran-besaran dalam Termodinamika
Usaha (W)
Menentukan Usaha (W) dapat dilakukan dengan rumus atau dengan Grafik P-V
1.Dengan rumus
W = p∆V= p(V2 – V1) Keterangan :
W = Usaha (J)
P = Tekanan (N/m²/Pa)
∆V = perubahan V, (V2 – V1)
2.Dengan Grafik P-V
W = luas daerah arsir

Gas memuai → W (+)
W = luas daerah arsir

Gas menyusut → W (-)
W = LUAS ABCD = ∆P . ∆V

Gas mengalami siklus
C. Hukum ke-0 Termodinamika
Jika benda A berada dalam kesetimbangan kalor dengan benda B dan benda B berada dalam kesetimbangan kalor dengan benda C, maka benda A berada dalam kesetimbangan kalor dengan benda C.
D. Hukum ke-1 Termodinamika
Hukum pertama termodinamika beranggapan bahwa energy bersifat kekal
Artinya :
Kalor yang diterima digunakan untuk membuat perubahan energy dalam /∆U, dimana ∆U = Ek = 3/2 kT dan untuk melakukan usaha W

E. Hukum ke-2 Termodinamika
Hukum kedua termodinamika berisi pernyataan tentang proses yang dapat / tidak dapat terjadi di alam dan tentang aliran kalor yang memiliki arah.
Hukum ini dijelaskan oleh 2 rumusan
- Rumusan Clausius

Agar kalor dapat mengalir dari reservoir (sumber bersuhu rendah ke tinggi), diperlukan W dari luar.
- Rumusan Kelvin – Planck
Kalor yang masuk tidak mungkin jadi usaha W seluruhnya, sebagian besar terbuang jadi Q2
F. Mesin Carnot
Di alam, tidak ada mesin yang berefisiensi sempurna, tetapi ada 1 mesin yang dirancang ideal. → ɳ - nya tinggi (mesin carnot). Karena ɳ tinggi → Q sebanding dengan T, sehingga Q₂/Q₁ = T₂/T₁.
Diagram P-V mesin Carnot

Besaran-besaran yang sering ditanyakan dalam mesin carnot adalah usaha (W), kalor yang dimasukkan (Q1), kalor yang terbuang (Q2), efisiensi mesin, suhu (T). Beberapa rumus di bawah ini adalah sebagian rumus cepat yang bisa digunakan untuk menyelesaikan soal terkait siklus carnot.


 G. Soal-soal
G. Soal-soal Volume suatu piston berubah dari 2 m3 menjadi 6 m3 pada tekanan 1 atm. Besarnya usaha yang dilakukan sistem adalah ....
- 100 kJ
- 200 kJ
- 400 kJ
- 500 kJ
- 600 kJ
Proses yang dilakukan sebuah gas pada ruang tertutup ditampilkan pada grafik P-V di bawah ini:
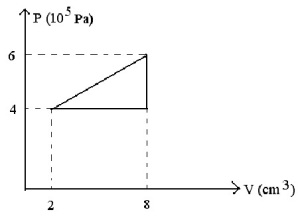
Besar usaha yang dilakukan gas per siklus adalah ....
- 0,12 J
- 0,60 J
- 1,20 J
- 6,00 J
- 12,0 J
Suatu mesin Carnot yang bekerja pada suatu reservoir suhu rendah 300 K memiliki efisiensi 50 %. Agar efisiensinya naik menjadi 80 %, reservoir suhu tinggi harus dinaikkan menjadi....
- 400 K
- 600 K
- 900 K
- 1000 K
- 1500 K
Sekian penjelasan singkat tentang materi termodinamika. Semoga membantu kita semua.
Salam (Stephanus)


Tidak ada komentar:
Posting Komentar